Chemistry Material for Groups Exams : రసాయన శాస్త్రంలో గ్రూప్స్ పరీక్షకు కీలకం.. మెండలీఫ్ ఆవర్తన పట్టికలోని గ్రూపులు ఎన్ని?

మాదిరి ప్రశ్నలు
ఇటీవల డిసెంబర్ 2018లో జరిగిన ఆర్ఆర్బీ పరీక్షల ప్రశ్నల సరళిని గమనిస్తే రసాయన శాస్త్రంలో అనువర్తిత అంశాలపై కాకుండా నేరుగా ప్రశ్నలు అడగడాన్ని గమనించవచ్చు. 8–10వ తరగతి పాఠ్యాంశాలపై అవగాహన ఉంటే సరిపోతుంది.
1. మెండలీఫ్ ఆవర్తన పట్టికలోని గ్రూపులు ఎన్ని?
1) 8 2) 8
3) 18 4) 14
జ: 2;
వివరణ: డాబర్నీర్, న్యూలాండ్స్, లోథర్మే యర్ల తర్వాత విస్తృతంగా మూలకాల వర్గీకరణ చేపట్టిన శాస్త్రవేత్త రష్యాకు చెందిన డిమిట్రీ మెండలీఫ్.
మెండలీఫ్ అప్పటికే కనుగొన్న 63 మూలకాలను, వాటి పరమాణు భారాల ఆరోహణ క్రమంలో అమర్చినప్పుడు, నిర్ధిష్ట వ్యవధులతో మూలకాల ధర్మాలు పునరావృతం కావడం గమనించాడు. దీని ఆధారంగానే ‘మూలకాల ధర్మాలు, వాటి పరమాణు భారాల ఆవర్తన ప్రమేయాలు’ అనే ఆవర్తన నియమాన్ని ప్రతిపాదించాడు.
మెండలీఫ్ ఆవర్తన పట్టికలో 7 పీరియడ్లు (అడ్డువరసలు), ఎనిమిది గ్రూప్లు (నిలువు గడులు) ఉన్నాయి.
2. కింది వాటిలో ఆవర్తన పట్టికలో భాగం కానివేవి?
1) హాలోజెన్లు 2) కార్సినోజెన్లు
3) లాంథనైడ్లు 3) ఆక్టినైడ్లు
జ: 2
వివరణ: 1, 3, 4లు ఆధునిక ఆవర్తన పట్టికలోని వివిధ కుటుంబాల పేర్లు. కార్సినోజెన్లు అంటే క్యాన్సర్ కారక సమ్మేళనాలు.
ఆవర్తన పట్టికలో వివిధ గ్రూపుల్లోని మూలకాలను, వాటి ధర్మాల ఆధారంగా వివిధ పేర్లతో వ్యవహరిస్తారు.
➾ మొదటి గ్రూప్ (IA లేదా 1)లోని మూలకాలు (Li, Na, K, Rb, Cs) ఆక్సైడ్లు నీటిలో కరిగి బలమైన క్షారాలనిస్తాయి. అందుకే వీటిని క్షార లోహాలు అంటారు.
➾ రెండో గ్రూపు (IIA లేదా 2) మూలకాలు (Be, Mg, Ca, Sr, Ba) ప్రకృతిలో స్వేచ్ఛా స్థితిలో లభిస్తాయి. వీటి ఆక్సైడ్లు ఉష్ణ స్థిరత్వం (వేడి చేసినా విఘటనం చెందని ధర్మం) కలిగి క్షార ధర్మాలను ప్రదర్శిస్తాయి. వీటిని క్షార మృత్తిక లోహాలు అంటారు.
☛Follow our YouTube Channel (Click Here)
➾ 15వ గ్రూప్ (15 లేదా VA) మూలకాలైన N, P, As, Sb, Biలను నిక్టోజన్లు అంటారు. గ్రీక్ భాషలో Pnico అంటే ఊపిరాడకుండా చేయు అని అర్ధం.
➾ 16వ గ్రూప్ (VIA) మూలకాలైన O, S, Se, Te, Poలను చాల్కోజన్లు అంటారు. అనేక మూలకాలు, ధాతువులు ఆక్సిజన్ లేదా సల్ఫర్ సమ్మేళనాలుగా ఉంటాయి. అందుకే వీటిని చాల్కోజన్లు (ధాతువులను ఏర్పరచేవి) అంటారు.
➾ 17వ గ్రూప్ (VIIA) గ్రూప్లోని F, Cl, Br, Iలను హాలోజన్లు అంటారు. వీటికి లవణాలను ఏర్పరిచే (హాలస్: లవణాలను ఏర్పర్చడం) గుణం ఉండటం వల్ల అలా పిలుస్తారు.
➾ 18వ గ్రూప్ (O గ్రూప్)నకు చెందిన He, Ne, Ar, Kr, Xe, Rnలకు చర్యాశీలత దాదాపుగా ఉండదు. అందుకే వీటిని∙జడవాయువులని అంటారు.
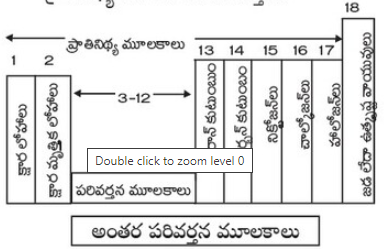
➾ ఆవర్తన పట్టికలో s-బ్లాక్, p-బ్లాకులను కలుపుతూ ఉన్న 10 గ్రూపుల మూలకాలను d-బ్లాక్ మూలకాలంటారు. వీటిలో జింకు గ్రూప్ తప్ప మిగిలిన మూలకాలను పరివర్తన మూలకాలంటారు. f- బ్లాక్ మూలకాలను అంతర పరివర్తన మూలకాలంటారు.
➾ ఇక జడవాయువులు, పరివర్తన, అంతర పరివర్తన మూలకాలు తప్ప మిగిలిన మూలకాలన్నిటిని ప్రాతినిథ్య మూలకాలని పిలుస్తారు.
3. ఒక మూలకం ఎలక్ట్రాన్ విన్యాసం 2, 8, 2. ఆధునిక ఆవర్తన పట్టికలో అదిచిచిచివ గ్రూప్నకు చెందుతుంది.
1) 5 2) 8 3) 2 4) 12
జ: 3;
☛ Follow our Instagram Page (Click Here)
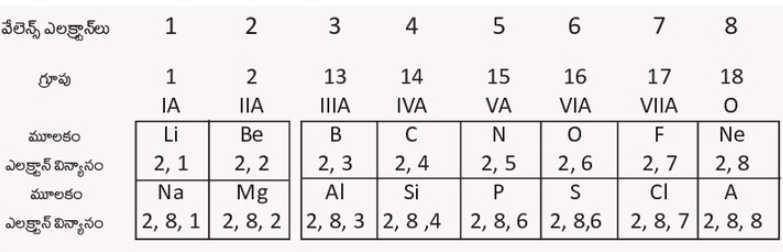
వివరణ: వివిధ కర్పరాల్లోని ఉపకర్పరాల్లో ఎలక్ట్రాన్ ఏ విధంగా వితరణ చెంది ఉన్నాయో ఎలక్ట్రాన్ విన్యాసం తెలియజేస్తుంది. వివిధ కక్ష్యల్లోని ఎలక్ట్రాన్ల సంఖ్యను ‘కామా’ గుర్తుతో వేరు చేస్తారు. చివరి కర్పరాల్లోని ఎలక్ట్రాన్లను వేలన్స్ ఎలక్ట్రాన్లు అంటారు. పై ప్రశ్నలో వేలన్స్ ఎలక్ట్రాన్ల సంఖ్య 2 కాబట్టి దీని గ్రూప్ సంఖ్య 2. వేలన్స్ ఎలక్ట్రాన్ల సంఖ్య ఆధారంగా గ్రూప్లను కింది వి«ధంగా గుర్తించవచ్చు.
4. కింది వాటిలో దేని పరమాణుకత ఒకటి?
1) ఆక్సిజన్ 2) ఆర్గాన్
3) హైడ్రోజన్ 4) సల్ఫర్
జ: 2
వివరణ: ఒక అణువులోని పరమాణువుల సంఖ్యను దాని పరమాణుకత అంటారు. వేర్వేరు మూలకాల పరమాణుకత వేర్వేరుగా ఉంటుంది.
➾ లోహాల పరమాణుకత ఒకటి (ఉదా: లిథియం, సోడియం, ఐరన్)
➾ జడవాయువుల పరమాణుకత ఒకటి (హీలియం, నియాన్, ఆర్గాన్, క్రి΄్టాన్, క్జినాన్, రేడాన్)
➾ ఆక్సిజన్, నైట్రోజన్, హైడ్రోజన్లతోపాటు హాలోజన్లు (ఫ్లోరిన్, క్లోరిన్, బ్రోమిన్, అయోడిన్)లు ద్విపరమాణుకాలు.
➾ ఓజోన్ పరమాణుకత – 3
➾ ఫాస్పరస్ పరమాణుకత – 4.
➾ సల్ఫర్ పరమాణుకత – 8.
5. 144గ్రా. మెగ్నీషియంలో ఉన్న గ్రామ్ పరమాణువుల సంఖ్య చిచిచిచి
1) 6 2) 144
3) 32 4) 64
జ: 1
వివరణ: మూలకాల పరమాణు భారాన్ని గ్రామ్లలో వ్యక్తపరిస్తే దాన్ని ఒక ‘గ్రామ్ పరమాణువు’గా పేర్కొంటారు.
ఉదా: Mg పరమాణుభారం 24 యూనిట్లు. కాబట్టి ఒక గ్రామ్ పరమాణువు మెగ్నీషియం = 24 గ్రామ్లు
24 గ్రా. మెగ్నీషియం = 1 గ్రామ్ పరమాణువు
144 గ్రా. మెగ్నీషియం
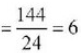 గ్రామ్ పరమాణువులు.
గ్రామ్ పరమాణువులు.
మరికొన్ని మూలకాల పరమాణు భారాలు (గ్రా) కింద ఇచ్చారు.
H C N O F Na Mg
1 12 14 16 17 23 24
AI P S Cl K Ca
23 31 32 35.5 39 40
☛ Join our WhatsApp Channel (Click Here)
6. NaCl∙ఫార్ములా యూనిట్ భారం?
1) 5.85 u 2) 58.5 u
3) 0.585 u 4) 584 u
వివరణ:
సోడియం (Na) పరమాణు భారం= 23

7. కింది వాటిలో క్షార ధర్మం కానిదేది?
1) ఎరుపు లిట్మస్ను నీలిగా మారుస్తుంది.
2) కొవ్వు పదార్ధాలను కరిగించుకుంటుంది.
3) నీటిలో హైడ్రోజన్ ఆయాన్లను ఇస్తుంది.
4) సబ్బు వంటి జారుడు గుణం ఉంటుంది.
జ: 3;
వివరణ: సాధారణంగా రుచికి పుల్లగా ఉన్నవి అమ్లాలు, సబ్బులాగా మృదువైన స్పర్శ ఉన్నవి క్షారాలు.
➾ అమ్లాలు నీలి లిట్మస్ను ఎరుపుగా, క్షారాలు ఎరుపు లిట్మస్ను నీలిగా మారుస్తాయి.
➾ అర్హినియస్ సిద్ధాంతం ప్రకారం అమ్లాలు నీటిలో హైడ్రోజన్ ఆయాన్లను, క్షారాలు హైడ్రాక్సిల్ ఆయాన్లను ఇస్తాయి.
➾ లోహాలు, లోహ ఆక్సైడ్లు నీటిలో కరిగి క్షారాలనిస్తాయి.(ఉదా: సోడియం ఆక్సైడ్, కాల్షియం ఆక్సైడ్)
➾ అలోహ అక్సైడ్లు నీటిలో కరిగి ఆమ్లాల నిస్తాయి.( ఉదా: సల్ఫర్, నైట్రోజన్, కార్బన్ ఆక్సైడ్లు)
➾ కొవ్వులను గాఢ క్షారాలతో కలిపి వేడిచేస్తే జలవిశ్లేషణ (స΄ోనిఫికేషన్) జరిగి సబ్బులు ఏర్పడతాయి.
➾ క్షారాలు ఫినాఫ్తలీన్ సూచికను పింక్ రంగుకు, మి«థైల్ ఆరెంజ్ సూచికను పసుపు రంగుకు మారుస్తాయి.
➾ ఆమ్లాలు మిథైల్ ఆరెంజ్ సూచికను నారింజ రంగుకు మారుస్తాయి. ఫినాఫ్తలీన్ రంగు చూపదు.
8. కింది వాటిలో సరికాని జత ఏది?
1) రక్తం pH : 7.4
2) వెనిగర్ pH : 2.2
3) శుద్ధమైన నీరు pH : 7.5
4) ΄ాలు pH : 6.6
జ: 2;
వివరణ: ఆమ్ల– క్షార బలాలను కొలవడానికి pH స్కేలును ఉపయోగిస్తారు. దీన్ని సొరెన్సెన్ అనే శాస్త్రవేత్త పరిచయం చేశాడు. హైడ్రోజన్ ఆయాన్ గాఢత రుణ సంవర్గమానాన్నే pHగా నిర్వచించారు.
pH= - log [H+]
అమ్ల ద్రావణం : pH < 7
తటస్థ ద్రావణం : pH = 7
క్షార ద్రావణం : pH > 7
కొన్ని సాధారణ ద్రవాల pH విలువలు కింది విధంగా ఉంటాయి.
☛ Join our Telegram Channel (Click Here)
| ద్రవం | pH | ధర్మం |
| గ్యాస్ట్రిక్ రసం | 1 – 2 | ఆమ్లం |
| ఆపిల్ రసం | 3.0 | ఆమ్లం |
| నిమ్మరసం | 2 – 3 | ఆమ్లం |
| వెనిగర్ | 2.2– 2.5 | ఆమ్లం |
| మూత్రం | 4.8– 7.5 | ఆమ్ల–క్షార |
| సోడా | 5.5 | ఆమ్లం |
| లాలాజలం | 6.4– 6.9 | ఆమ్లం |
| పాలు | 6.6– 6.8 | ఆమ్లం |
| బ్లాక్ కాఫీ | 5.0 | ఆమ్లం |
| టోమాటో రసం | 4.5 | ఆమ్లం |
| వర్షపు నీరు | 6.5– 6.9 | ఆమ్లం |
| స్వచ్ఛమైన నీరు | 7 | తటస్థం |
| రక్తం | 7.3– 7.4 | క్షారం |
| కన్నీరు | 7.4 | క్షారం |
Tags
- chemistry bit banks
- groups exams preparations
- Competitive Exams
- chemistry groups exams
- material/bit banks for chemistry groups exams
- appsc and tspsc groups
- appsc and tspsc chemistry bit banks
- police jobs based exams
- government jobs with groups exams
- group exams study material and bit banks
- chemistry material and bit banks for groups exams
- Education News
- Sakshi Education News
- chemistrystudymaterials




















